MitraClip®の予後改善効果 MITRA-FRとCOAPT
NEJMoa1806640
・ESC2018でMITRA-FR (NEJMoa1805374) が発表され、MitraClipにnegativeな結果が報告されてから僅か一ヶ月、TCT2018で発表されたCOAPT(NEJMoa1806640)は対象的にpositiveな結果でした。どちらも二次性僧帽弁逆流症を対象としたMitraClipと薬物療法のRCTです。
 MITRA-FR
MITRA-FR
 COAPT
COAPT
・MITRA-FR:1年フォローアップで全死亡と心不全入院の複合エンドポイントに有意差なし
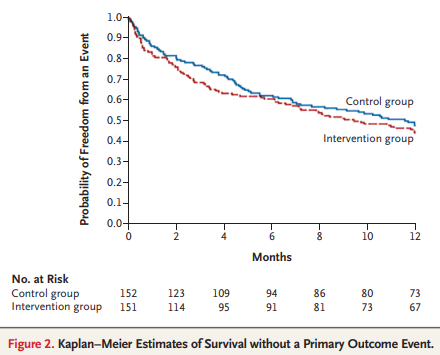
・COAPT:2年フォローアップで年間心不全入院率はMitraClip群35.8%/年、コントロール群67.9%/年 (HR 0.53; 95% CI 0.40 to 0.70; P<0.001). 2年全死亡率はMitraClip群29.1%、コントロール群46.1%(HR 0.62; 95% CI, 0.46 to 0.82; P<0.001).
・上記のようにかなり違った結果になりました。きっとデザインや患者背景に大きな違いあるのではというとそれほどでもなく、TCTでも議論を呼んだようです
・おおよその患者背景を比較してみます
MITRA-FR(左):平均年齢70歳、虚血性心筋症が6割、NYHAⅡが3割、NYHAⅢが5-6割、EF33%、LVEDVi 135ml/m2、MRのEROA31mm2、NT-proBNP 3400ng/L、BNP800ng/L
COAPT(右):平均年齢72歳、虚血性心筋症が6割、NYHAⅡが4割、NYHAⅢが5割、EF31%、LVEDVi 101ml/m2、MRのEROA41mm2、NT-proBNP 5100~5900ng/L、BNP1000ng/L

・COAPTの方がMRは重症だがEDVの保たれた患者が多い印象です
・他に、MITRA-FRと比較してCOAPTでは
・最大薬物療法を厳格に行ってからenrollする
・そのため試験期間が長期化し、術者が手技に熟達した
などの点が良い成績につながったのではと、COAPTの1st authorであるDr. Stoneのインタビュー(上記リンク)で触れられていました。
・また、MITRA-FRではAbbottの関与はデバイス提供などに限られデータ解析には一切関わってないようです(page 27, Supplementary Appendix, NEJMoa1805374)が、COAPTではdata management, analysis, monitoringをAbbottが担っています(page4, Supplementary Appendix, NEJMoa1806640)。
・纏めると、secondary MRに対するMitraClipは、患者選択をきちんと行うことが重要そうだが、具体的にどのような群が最も恩恵を受けるのかはまだ分からない、と言えそうです。下に示すように、COAPTのサブルグープ解析はその答えを教えてはくれなさそうです。
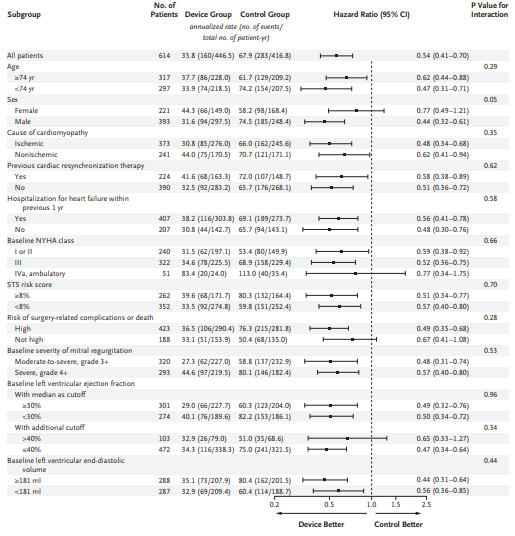
・より大規模なRESHAPE-HF試験が進行中で、その結果が待たれます。各試験の比較はこちら(JACC Mar 2015, 65 (12) 1231-1248)
High-risk patientでのCoreValveの5年成績(TCT2018)

(引用:JACC Sep 2018, 25522; DOI:10.1016/j.jacc.2018.08.2146)
・1年成績を比較した試験()ではTAVRの優位性が示されていましたが、5年後ではほぼ同等という結果。
・TAVRの方がペースメーカーが多かったのは変わらず。
・弁の劣化や変性は、5年ではSAVRと変わりないと考えて良さそう。
ACSにおけるスタチンローディング(SECURE-PCI)
Effect of Loading Dose of Atorvastatin Prior to Planned Percutaneous Coronary Intervention on Major Adverse Cardiovascular Events in Acute Coronary Syndrome
■デザイン:多施設ランダム化二重盲検プラセボ比較施設
■背景:ACSにおけるスタチンのローディングに関して既存の報告はサンプル数が少ないなどエビデンスが限られている
■Population:ブラジルの、ACSの診断で7日間以内に侵襲的治療を受けた患者4191人
■介入:アトルバスタチン80mg*2回 VS プラセボ
※STEMIでは可及的速やかに1回目を投与、24時間後に2回目、それ以外ではCAGの12時間前と2時間前に投与
※その後は、全患者でアトルバスタチン40mg/dayを最低30日間継続
■一次アウトカム:30日MACE(全死亡、急性心筋梗塞、脳梗塞、予定外の再血行再建の複合アウトカム)
■結果:N=4191, 平均年齢 61.8歳、女性は25.9%、30日脱落率は0.7%。64.7%がPCI, 8%がCABG、27.3%が薬物療法を選択。30日MACEはアトルバスタチン群で6.2%、プラセボ群で7.1%(absolute difference, 0.85%[95%CI, −0.70%to 2.41%]; hazard ratio, 0.88; 95%CI, 0.69-1.11; P = .27).
■結論:ACSにおけるスタチンのローディングは 30日MACEを減少させなかった。
感想:
・…という試験なのですが、サブグループ解析が印象的です。
・PCI群に限ると、30日MACEがアトルバスタチン群(n=417)で約7%、プラセボ群(n=448)で約13%と、大きく差が付きました(HR, 0.54; 95% CI, 0.35-0.84; P = .01)。NNT≒16と考えると凄いですね。

(引用:)
・なお、NSTEMIや非PCI群では有意差はありませんでした。
・本研究ではSTEMI, NSTEMI, uAPや、PCI, CABG, OMTが混在しているため有意差がつかなかったものと思われますが、STEMIに対しPCIを行う場合に限ってはスタチンローディングが有効かも知れません。
・MACEの内訳を見ると全体的にスタチン群が低い傾向ですが、はっきり差がついたのはnon-PCI siteのMIでした。ステントの開存性よりも、スタチンのpleiotropic effectsが血管炎症など色々な面でじわっと効いているんでしょうか。
・CABG群に限ると…?記載がありませんでした。本研究ではCABG群が333名と少なく、結論は出なさそうです。
・なお「STEMIにPCIを行う症例」でスタチンローディングの効果を調べたSTATIN-STEMI trial(JACC Cardiovasc Interv. 2012 Feb;5(2):248.)では、80mgローディングでイベント減少傾向が見られましたが有意差は付きませんでした。ただしn=171とサンプル不足だっった可能性があります。
・強く躊躇う理由がないので、個人的にはSTEMIでは出来るだけ早く高用量のストロングスタチンを入れるようにしており、その思いが強くなりました。
・また「FHの疑い」病名をつければ日本の保険診療でもアトルバスタチン40mgやロスバスタチン20mgのローディングまでは可能かな?と思ったりしていますが、今の所そこまでは実行せずにいます。
アスピリンは健常高齢者の二次予防に有効か?(ASPREE trial)
Effect of Aspirin on Disability-free Survival in the Healthy Elderly
https://www.nejm.org/doi/full/10.1056/NEJMoa1800722
■デザイン:ランダム化二重盲検プラセボ比較試験
■背景:心血管疾患の既往の無い高齢者へのアスピリンの一次予防効果があるかは定かではない
■Population:米国34施設、豪州14施設の患者から、70歳以上(黒人とヒスパニックは65歳以上)の患者を抽出し被験者を募った。n=19114。除外基準は心血管疾患、心房細動のほか、認知症、貧血、余命5年を期待できない併存症など
■一次アウトカム:Disability-free Survival ※死亡、認知症、身体活動制限の複合アウトカム
■結果:アスピリン継続の意義がないと考えられ4.7年(当初6年の予定)で打ち切り。一次アウトカムはアスピリン群で21.5/1000 人年、プラセボ群で21.2/1000人年 (hazard ratio, 1.01; 95% confidence interval [CI], 0.92 to 1.11; P = 0.79)。ただし出血はアスピリン群で有意に多かった(3.8% vs. 2.8%; hazard ratio, 1.38; 95% CI, 1.18 to 1.62; P<0.001)。
■結論:アスピリンを健常高齢者に用いることはDisability-free survivalを延長せず、出血イベントを増加させた
 (引用:https://www.nejm.org/doi/full/10.1056/NEJMoa1800722)
(引用:https://www.nejm.org/doi/full/10.1056/NEJMoa1800722)
感想:
・まず気になるのが「健康な高齢者」がどれくらい心血管リスク因子を持っていたかですが、介入群と対照群で僅かな(1%程度の)差こそあれ、喫煙はcurrent smokerが4%(!)、ex-smokerが約40%、糖尿病10%、高血圧75%、脂質異常症65%程度とのことでした。
・また、PPIやH2ブロッカーの併用状況ですが、組み入れ時にはPPIが25%、H2RBが2%とであり、その後どうしたかは記載がありませんでした
・アスピリンの一次予防効果における既存の報告は、海外では50~74歳を対象とした否定的なメタ解析(Lancet 2009;373:1849-1860)が、国内では85歳以下の2型DM患者を対象としたJPAD(JAMA. 2008;300:2134-41)や60歳以上で心血管リスクを持つが既往のない患者を対象としたJPPP(JAMA 2014;312: 2510-20)があり、いずれも、せいぜい僅かな心血管疾患予防効果が見られたものもあれど、出血と相殺しあうなどして総合的には優位性なしという結果ばかりでした。
・胃粘膜保護薬と併用するのは…?polypharmacyや、PPIの長期投与の有害性が指摘されていることなど考えると、一次予防でそれは普通は無いなと思います。
・個人的には、よっぽど心血管リスクが高かったりなど特別な理由があれば一次予防での使用も考慮するものの、単にリスク因子が1-2個あるだけではアスピリンは使用せずリスク因子への介入のみにしています(当然?)。
ワーファリンが良好にコントロールされていれば、その後も良好なコントロールが期待できるか?
JACC, 2018 Volume 72, Issue 12, Pages 1357-1365,
■デザイン:後ろ向きコホート研究
■背景:AFに対しVKAを使用中のPtで、現行ガイドライン(ESCやNICE)ではTime in therapeutic range(TTR: 定期的な検査でINRが治療域にある割合) が70%以下の場合にDOACへの変更を推奨しているが、70%を超えた群でDOACへの変更が良いかは決まっていない。そのためTTRが70以上の患者での塞栓イベントや出血イベントのリスクについて研究した。
■方法:Danish National Patient Registry(デンマーク全土の入院レジストリ), Danish Presription Registry(デンマーク内の処方情報), Danish Civil Registration System(全国民の生死の状況). からデータを取得。1997年1月1日から2011年8月22日までにAFに対しVKAが処方された患者18415名のうち、6ヶ月間継続しており、Exclusion criteria (半年で採血が3回未満、50日以上採血感覚が開いている、弁膜症性AFなど)に該当しなかった患者4772名について転機を調べた
Inclusionの際の各群のn数は以下の通り。採血と採血の間の期間のINRは直線的に変動したものと家庭してTTRを計算した。
■結果:TTR ≧70%の患者で 12ヶ月後も70%を超えていたのは513名 (55.7%) 。また当初のTTRが70%未満であることは、stroke/thromboembolism(HR: 1.14; 95% confidence interval [CI]: 0.77 to 1.70) やmajor bleeding (HR: 1.12; 95% CI: 0.84 to 1.49)とは相関しなかった 。
■結論:AFに対しVKAを使用している患者は、 TTR ≧70% であったとしてもその翌年には半数が70%を下回っており、TTRは良好な管理の予測指標にはならない。

(引用:http://www.onlinejacc.org/content/72/12/1357)
Central Illustration:組み入れ時にINRコントロール良好(TTR≧70%)であった患者も、その後1年以内に約半数が70%を下回る(左図)。また、組入時のTTRはStroke/thromboembolism, Major bleedingのいずれとも相関しなかった
感想
・もともとワーファリンを飲んでいてコントロール良好なら「別にDOACにする必要もないかな」と考えてワーファリンを継続する、ということは良くあると思いますが、そうとも限らないのでは?という論文(ワーファリン開始わずか半年のコントロールで層別化しているので、厳密には少し違います)
・当初のコントロールが良くても、その後コントロール不良になる可能性が50%近い、というのは感覚より少し多い印象です。
・当然ですが「その後のコントロールも良好であった群では塞栓や出血のイベントが少なかった」ともあるので、頻回にモニタリングして結果的に良好なコントロールが維持できている人は大丈夫なんでしょう
・しかし病診連携の昨今、急性期病院の先生は患者さんを手放すことが多いでしょうし、クリニックの先生は多忙な外来のなかで頻回の調整はなかなか難しいこともあるでしょうから、「きちんと気をつけてれば大丈夫なんでしょ」とも簡単には言えないなぁと思いした。
※本論文での「良好なコントロール」は欧米なので一律INR2.00-3.00と定義されているようです。敢えて低めにコントロールされた患者も含まえているかも知れません。